Advertisements
Advertisements
Question
विभिन्न तापों पर N2O5 के अपघटन के लिए वेग स्थिरांक नीचे दिए गए हैं –
| T/°C | 0 | 20 | 40 | 60 | 80 |
| 105 × k/s–1 | 0.0787 | 1.70 | 25.7 | 178 | 2140 |
In k एवं 1/T के मध्य ग्राफ खींचिए तथा A एवं Ea की गणना कीजिए। 30°C तथा 50°C पर वेग स्थिरांक को प्रागुक्त कीजिए।
Advertisements
Solution
विभिन्न तापमानों पर N2O5 के अपघटन के दर स्थिरांक नीचे दर्शाए गए हैं।
| T(°C) | T(K) | 1/T | k(s−1) | In k (= 2.303 log k) |
| 0 | 273 | 3.6 × 10−3 | 7.87 × 10−7 | −14.06 |
| 20 | 293 | 3.4× 10−3 | 1.70 × 10−5 | −10.98 |
| 40 | 313 | 3.19 × 10−3 | 25.7 × 10−5 | −8.266 |
| 60 | 333 | 3.00 × 10−3 | 178 × 10−5 | −6.332 |
| 80 | 353 | 2.8 × 10−3 | 2140 × 10−5 | −3.844 |
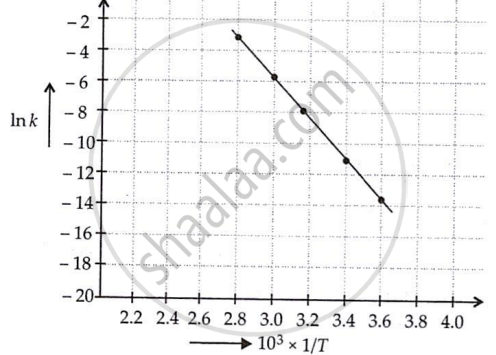
रेखा का ढलान = tan θ
= `("y"_2 - "y"_1)/("x"_2 - "x"_1)`
= `(-10.98-(-14.06))/(3.4 - 3.6) xx 10^3`
= −15.5 × 103
Ea = −ढलान × R
= −(−15.5 × 103 × 8.314)
= 128.86kJ K−1 mol−1
पुनः A में = k में + `"E"_"a"/("RT")`
= `-14.06 + (128.86 xx 10^3 "JK"^(-1) "mol"^(-1))/(8.314 xx 273)`
= −14.06 + 56.77
= 42.71
या, log A = 18.53
या, A = antilog 18.53 = 0.3388 × 1019
या, A = 3.3888 × 1018
303 K और 323 K पर दर स्थिरांक k के मान ग्राफ से प्राप्त किए जा सकते हैं।
सबसे पहले, `1/(303"K") और 1/(323"K")` के अनुरूप k प्राप्त किया जाता है और फिर k की गणना की जाती है।
APPEARS IN
RELATED QUESTIONS
ताप में 293 K से 313 K तक वृद्धि करने पर किसी अभिक्रिया का वेग चार गुना हो जाता है। इस अभिक्रिया के लिए सक्रियण ऊर्जा की गणना यह मानते हुए कीजिए कि इसका मान ताप के साथ परिवर्तित नहीं होता।
गलत कथनों को चिह्नित कीजिए।
- उत्प्रेरक अभिक्रिया को वैकल्पिक पथ उपलब्ध कराता है।
- उत्प्रेरक सक्रियण ऊर्जा को बढाता है।
- उत्प्रेरक सक्रियण ऊर्जा को कम करता है।
- उत्प्रेरक अभिक्रिया के एन्थैल्पी परिवर्तन को बदल देता है।
निम्नलिखित में से कौन-सा कथन अरेनियस समीकरण के अनुसार है?
- ताप में वृद्धि के साथ अभिक्रिया का वेग बढता है।
- सक्रियण ऊर्जा में कमी के साथ अभिक्रिया का वेग बढ़ता है।
- ताप में वृद्धि के साथ वेग स्थिरांक में चरघतांकी कमी होती है।
- सक्रियण ऊर्जा में कमी से अभिक्रिया का वेग घटता है।
ऊजा के वितरण को दशाने वाले मैक्सवेल बोल्ट्जमान द्वारा दिए ग्राफ में ______।
- ताप में वृद्ध के साथ वक्र के अंतर्गत क्षेत्रफल स्थिर रहना चाहिए।
- ताप में वृद्ध के साथ वक्र के अंतर्गत क्षेत्रफल बढ़ता है।
- ताप में वुद्ध के साथ वक्र के अंतर्गत क्षेत्रफल घटता है।
- ताप में वृद्ध के साथ वक्र चौड़ा हो जाता है तथा दाहिनी ओर विस्थापित हो जाता है।
स्पष्ट कीजिए कि H2(g) तथा O2(g) के मध्य अभिक्रिया अति संभाव्य है परन्तु गैसों को एक ही पात्र में कमरे के ताप पर रखने से जल क्यों नहीं बनता।
कक्ष ताप पर वायु में ऑक्सीजन प्रचुरता से उपलब्ध होने पर भी ईंधन स्वयं क्यों नहीं जलते?
तीन से अधिक आणिकता वाली अभिक्रियाओं की संभावनाएँ बहुत कम क्यों होती हैं?
किसी अभिक्रिया के लिए केवल ऊष्मागतिक संभाव्यता अभिक्रिया के वेग को निर्धारित नहीं कर सकती। इसे एक उदाहरण की सहायता से समझाइए।
ऑक्सैलिक अम्ल तथा KMnO4 के मध्य ऑक्सीकरण-अपचयन अनुमापन में हम अनुमापन प्रारम्भ करने से पूर्व ऑक्सैलिक अम्ल विलयन को गरम क्यों करते हैं?
किसी अभिक्रिया के वेग नियम को हम संतुलित रासायनिक अभिक्रिया की सहायता से निर्धारित क्यों नहीं कर सकते?
