Advertisements
Advertisements
प्रश्न
Advertisements
उत्तर
(i) [Co(NH3)6]3+
(iii) [Fe(CN)6]4–
स्पष्टीकरण:
(i) Co3+ का [Co(NH3)6]3+ में आण्विक कक्षीय इलेक्ट्रॉनिक विन्यास -
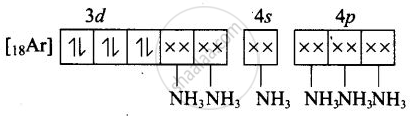
अयुग्मित इलेक्ट्रॉनों की संख्या = 0
चुंबकीय गुण = प्रतिचुंबकीय
(ii) Mn3+ का [Mn(CN)6]3– में आण्विक कक्षीय इलेक्ट्रॉनिक विन्यास -
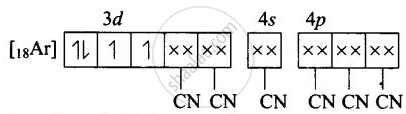
अयुग्मित इलेक्ट्रॉनों की संख्या = 2
चुंबकीय गुण = अनुचुंबकीय
(iii) Fe2+ का [Fe(CN)6]4– में आण्विक कक्षीय इलेक्ट्रॉनिक विन्यास -
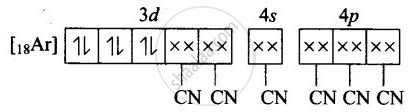
अयुग्मित इलेक्ट्रॉनों की संख्या = 0
चुंबकीय गुण = प्रतिचुंबकीय
(iv) Fe3+ का [Fe(CN)6]3– में आण्विक कक्षीय इलेक्ट्रॉनिक विन्यास -
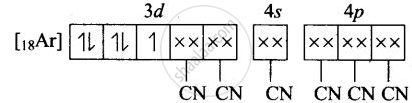
अयुग्मित इलेक्ट्रॉनों की संख्या = 1
चुंबकीय गुण = अनुचुंबकीय
APPEARS IN
संबंधित प्रश्न
उपसहसंयोजन यौगिकों का रंग क्रिस्टल क्षेत्र विपाटन पर निर्भर करता है। संकुलों [Co(NH3)6]3+, [Co(CN)6]3− तथा [Co(H2O)6]3+ का दृश्य क्षेत्र में तरंगदैर्घ्य के अवशोषण का सही क्रम क्या होगा?
अष्टफलकीय [CoCl6]4− के लिए CFSE 18,000 cm−1 है, तो चतुष्फलकीय [CoCl4]2− की CFSE होगी ______।
[Fe(CN)6]3– संकुल के विषय में कौन-से विकल्प सही हैं?
(i) d2sp3 संकरण
(ii) sp3d2 संकरण
(iii) अनुचुंबकीय
(iv) प्रतिचुंबकीय
कोबाल्ट (II) क्लोराइड के गुलाबी रंग के जलीय विलयन में आधिक्य में HCl मिलाने से यह गहरे नीले रंग का हो जाता है। ऐसा इसलिए होता है क्योंकि
(i) [Co(H2O)6]2+ का [CoCl6]4− में परिवर्तन होता है।
(ii) [Co(H2O)6]2+ का [CoCl4]2− में परिवर्तन होता है।
(iii) चतुष्फलकीय संकुलों का क्रिस्टल क्षेत्र विपाटन अष्टफलकीय संकुलों की तुलना में कम होता है।
(iv) चतुष्फलकीय संकुलों का क्रिस्टल क्षेत्र विषाटन अष्टफलेकीय संकुलों की तुलना में अधिक होता है।
निम्न प्रचक्रण चतुष्फलकीय संकुल क्यों नहीं बनते?
क्रिस्टल क्षेत्र विपाटन सिद्धांत का प्रयोग करते हुए ऊर्जा स्तर आलेख बनाइए और निम्नलिखित में केंद्रीय धातु परमाणु/आयन का इलेक्ट्रॉनी विन्यास लिखकर चुंबकीय आघूर्ण का मान निर्धारित कीजिए।
[CoF6]3–, [Co(H2O)6]2+, [Co(CN)6]3–
संयोजकता आबंध सिद्धांत द्वारा [Mn(CN)6]3− के संबंध में निम्नलिखित को स्पष्ट कीजिए।
- संकरण का प्रकार
- आंतरिक अथवा बाह्य कक्षक संकुल
- चुंबकीय व्यवहार
- केवल प्रचक्रण चुंबकीय आघूर्ण मान
संयोजकता आबंध सिद्धांत द्वारा [FeCl6]4− के संबंध में निम्नलिखित को स्पष्ट कीजिए।
- संकरण का प्रकार
- आंतरिक अथवा बाह्य कक्षक संकुल
- चुंबकीय व्यवहार
- केवल प्रचक्रण चुंबकीय आघूर्ण मान
