Advertisements
Advertisements
Question
निकाय \[\ce{Mg^{2+} | Mg}\] का मानक इलैक्ट्रोड विभव आप किस प्रकार ज्ञात करेंगे?
Advertisements
Solution
निकाय \[\ce{Mg^{2+} | Mg}\] का मानक इलैक्ट्रोड विभव ज्ञात करने के लिए एक सेल स्थापित करते हैं। जिसमें एक इलैक्ट्रोड \[\ce{Mg | MgSO4 (1 M)}\], एक मैग्नीशियम के तार को \[\ce{(1 M) MgSO4}\] विलयन में डुबोकर व्यवस्थित करते हैं तथा मानक हाइड्रोजन इलैक्ट्रोड \[\ce{Pt}\], \[\ce{H2 (1 atm) | H+ (1 M)}\] को दूसरे इलैक्ट्रोड की भाँति व्यवस्थित करते हैं।
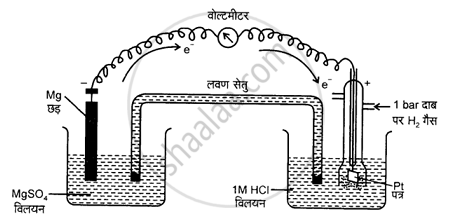
सेल का विद्युत वाहक बल मापते हैं तथा वोल्टमीटर में विक्षेप की दिशा को भी नोट करते हैं। विक्षेप की दिशा प्रदर्शित करती है कि इलेक्ट्रॉनों को प्रवाह मैग्नीशियम इलैक्ट्रोड से हाइड्रोजन इलैक्ट्रोड की ओर है। अर्थात् मैग्नीशियम इलैक्ट्रोड पर ऑक्सीकरण तथा हाइड्रोजन इलैक्ट्रोड पर अपचयन होता है। अत: सेल को निम्नवत् व्यक्त किया जा सकता है –
\[\ce{Mg | Mg^{2+} (1 M) || H+ (1 M) | H2 (1 atm), Pt}\]
\[\ce{E^Θ_{{सेल}} = E^Θ_{{H^{+}}/{{H_2}}} - E^Θ_{{Mg^{2+}/ Mg}}}\]
परंतु \[\ce{E^Θ_{{H^{+}}/{{H_2}}}}\] = 0
अत: \[\ce{E^Θ_{{Mg^{2+}/Mg}}}\] = \[\ce{- E^Θ_{{सेल}}}\]
यह देखा गया कि सेल का EMF 2.36 V है।
इसलिए, \[\ce{Mg^{2+} | Mg}\] प्रणाली के लिए मानक इलेक्ट्रोड विभव EΘ = −2.36 V होगा।
APPEARS IN
RELATED QUESTIONS
मानक इलैक्ट्रोड विभव की तालिका का निरीक्षण कर तीन ऐसे पदार्थ बताइए जो अनुकूल परिस्थितियों में फेरस आयनों को ऑक्सीकृत कर सकते हैं।
निम्नलिखित अभिक्रिया वाले गैल्वैनी सेल का मानक सेल-विभव परिकलित कीजिए।
\[\ce{2Cr_{(s)} + 3Cd^{2+}_{( aq)} -> 2Cr^{3+}_{( aq)} + 3Cd}\]
उपर्युक्त अभिक्रिया के लिए ΔrGΘ एवं साम्य स्थिरांकों की भी गणना कीजिए।
निम्नलिखित अभिक्रिया वाले गैल्वैनी सेल का मानक सेल-विभव परिकलित कीजिए।
\[\ce{Fe^{2+}_{( aq)} + Ag^+_{( aq)} -> Fe^{3+}_{( aq)} + Ag_{(s)}}\]
उपर्युक्त अभिक्रिया के लिए ΔrGΘ एवं साम्य स्थिरांकों की भी गणना कीजिए।
