Advertisements
Advertisements
प्रश्न
निम्नलिखित अरेनियस समीकरण पर विचार कीजिए और सही विकल्प पर निशान लगाइए।
κ = `"Ae"^(-"E"_"a"//"RT")`
पर्याय
अभिक्रिया स्थिरांक बढุती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से बढ़ता है।
अभिक्रिया स्थिरांक बढุती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से कम होता है।
अभिक्रिया दर स्थिरांक घटती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से बढ़ता है।
अभिक्रिया दर स्थिरांक घटती सक्रियण ऊर्जा और बढ़ते ताप के साथ चरघातांक से बढ़ता है।
Advertisements
उत्तर
अभिक्रिया दर स्थिरांक घटती सक्रियण ऊर्जा और बढ़ते ताप के साथ चरघातांक से बढ़ता है।
स्पष्टीकरण -
κ = `"Ae"^(-"E"_"a"//"RT")`
समीकरण से यह स्पष्ट है कि दर स्थिरांक k का मान सक्रियण ऊर्जा Ea में कमी और तापमान में वृद्धि के साथ तेजी से बढ़ता है।
जैसे-जैसे Ea घटता है, `(-"E"_"a"//"RT")` बढ़ता है और k बढ़ता है
जैसे-जैसे T बढ़ता है, `(-"E"_"a"//"RT")` घटता है और `(-"E"_"a"//"RT")` बढ़ता है और k बढ़ता है।
APPEARS IN
संबंधित प्रश्न
वेग स्थिरांक पर ताप का क्या प्रभाव पड़ता है? ताप के इस प्रभाव को मात्रात्मक रूप में कैसे प्रदर्शित कर सकते हैं?
विभिन्न तापों पर N2O5 के अपघटन के लिए वेग स्थिरांक नीचे दिए गए हैं –
| T/°C | 0 | 20 | 40 | 60 | 80 |
| 105 × k/s–1 | 0.0787 | 1.70 | 25.7 | 178 | 2140 |
In k एवं 1/T के मध्य ग्राफ खींचिए तथा A एवं Ea की गणना कीजिए। 30°C तथा 50°C पर वेग स्थिरांक को प्रागुक्त कीजिए।
किसी अभिक्रिया \[\ce{A -> {उत्पाद}}\] के लिए k = 2.0 × 10−2 s−1 है। यदि A की प्रारंभिक सांद्रता 1.0 mol L−1 हो तो 100 s पश्चात् इसकी सांद्रता क्या रह जाएगी?
हाइड्रोकार्बन का विघटन निम्न समीकरण के अनुसार होता है। Ea की गणना कीजिए।
k = `(4.5 xx 10^11 "s"^-1) "e"^(-28000 "K"//"T")`
ताप में 293 K से 313 K तक वृद्धि करने पर किसी अभिक्रिया का वेग चार गुना हो जाता है। इस अभिक्रिया के लिए सक्रियण ऊर्जा की गणना यह मानते हुए कीजिए कि इसका मान ताप के साथ परिवर्तित नहीं होता।
निम्नलिखित में से कौन-सा ग्राफ ऊष्माक्षेपी अभिक्रिया को प्रदर्शित करता है-
(क)
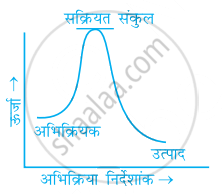
(ख)
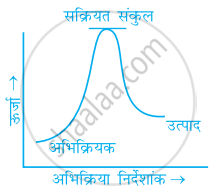
(ग)
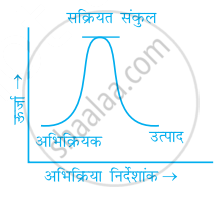
गलत कथनों को चिह्नित कीजिए।
- उत्प्रेरक अभिक्रिया को वैकल्पिक पथ उपलब्ध कराता है।
- उत्प्रेरक सक्रियण ऊर्जा को बढाता है।
- उत्प्रेरक सक्रियण ऊर्जा को कम करता है।
- उत्प्रेरक अभिक्रिया के एन्थैल्पी परिवर्तन को बदल देता है।
ऊर्जा के मैक्सवेल बोल्ट्जमान वितरण के अनुसार ______।
- उच्च तापों पर अधिकतम सम्भाव्य गातिज ऊर्जा प्राप्त अणुओं का अंश घटता है।
- उच्च तापों पर अधिकतम सम्भाव्य गातिज ऊर्जा प्राप्त अणुओं का अंश बढ़ता है।
- उच्च तापों पर अधिकतम सम्भाव्य गतिज ऊर्जा बढ़ती है।
- उच्च तापों पर अधिकतम सम्भाव्य गतिज ऊर्जा घटती है।
ताप में वृद्ध से अभिक्रिया वेग क्यों बढ़ता है?
किसी अभिक्रिया के वेग नियम को हम संतुलित रासायनिक अभिक्रिया की सहायता से निर्धारित क्यों नहीं कर सकते?
