Advertisements
Advertisements
Question
क्यों डाइऑक्सीजन एक गैस है, जबकि सल्फर एक ठोस है?
Advertisements
Solution
ऑक्सीजन pπ – pπ बहुल बंध बनाता है। छोटे आकार तथा उच्च विद्युत ऋणात्मकता के कारण ऑक्सीजन द्विपरमाणुक अणु (O2) के रूप में पाया जाता है। ये अणु परस्पर दुर्बल वाण्डर वाल्स आकर्षण बलों द्वारा जुड़े रहते हैं जो कमरे के ताप पर अणुओं के संघट्टों द्वारा सरलता से हट जाते हैं। अत: O2 कमरे के ताप पर एक गैस होती है।
सल्फर अपने विशाल आकार तथा कम विद्युत ऋणात्मकता के कारण pπ – pπ बहुल बंध नहीं बनाता है, अपितु यह S – S एकल बंध बनाते हैं। पुनः O – O एकल बंधों से अधिक प्रबल S – S बंधों के कारण सल्फर में श्रृंखलन का गुण ऑक्सीजन से अधिक होता है। अत: सल्फर श्रृंखलन की उच्च प्रवृत्ति तथा pπ – pπ बहुल बंध बनाने की अल्प प्रवृत्ति के कारण अष्टपरमाणुक अणु (S8) बनाता है जिसकी संकुचित वलय संरचना (puckered ring structure) होती है। विशाल आकार के कारण S8 अणुओं को परस्पर बाँधे रखने वाले आकर्षण बल पर्याप्त प्रबल होते हैं जिन्हें कमरे के ताप पर अणुओं के संघट्टों द्वारा नहीं हटाया जा सकता है। अत: सल्फर कमरे के ताप पर एक ठोस होता है।
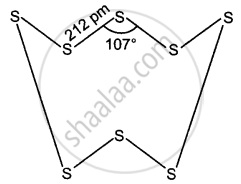
सल्फर अणु (S8)
