Advertisements
Advertisements
प्रश्न
ऐरिल हैलाइड ऐल्किल हैलाइडों की अपेक्षा नाभिकरागी प्रतिस्थापन के प्रति कम क्रियाशील क्यों होते हैं? हम ऐरिल हैलाइडों की क्रियाशीलता कैसे बढ़ा सकते हैं?
Advertisements
उत्तर
ऐरिल हैलाइड नाभिकरागी प्रतिस्थापन अभिक्रियाओं के प्रति निम्नलिखित कारणों से कम क्रियाशील होते हैं।
(i) हैलोऐरीन में हैलोजन परमाणु पर उपस्थित एकाकी इलेक्ट्रॉन युगल वलय के π इलेक्ट्रॉनों के साथ संयुग्मन में होते हैं तथा निम्नलिखित अनुनादी संरचनाएँ संभव हैं।
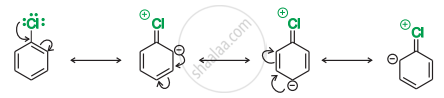
अनुनाद के कारण C-Cl आबंध में आंशिक द्विबंध के गुण आ जाते हैं। जिसके परिणामस्वरूप हैलोऐल्केन की तुलना में हैलोरीन में आबंध विदलन अपेक्षाकृत कठिन होता है। अत: ये नाभिकरागी प्रतिस्थापन अभिक्रियाओं के प्रति कम क्रियाशील होती हैं।
(ii) हैलोऐल्केन में हैलोजन से जुड़ा कार्बन परमाणु sp3 संकरित होता हैं जबकि हैलोऐरीन में हैलोजन परमाणु से जुड़ा कार्बन परमाणु sp2 संकरित होता है।
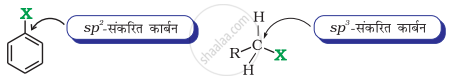
अधिक s गुणयुक्त sp2 संकरित कार्बन अधिक विद्युतऋणात्मक होता है तथा हैलोऐल्केन में कम s गुण युक्त sp3 संकरित कार्बन परमाणु की तुलना में C-X आबंध के इलेक्ट्रॉन युगल को अपेक्षाकृत अधिक सुदृढ़ता से थाम सकता है।अतः हैलोऐल्केन में C-Cl आबंध की लंबाई 177 pm, है जबकि हैलोऐरीन में 169 pm है। चूँकि लंबे बंध की तुलना में छोटे बंध को तोड़ना कठिन होता है, अतः नाभिकरागी प्रतिस्थापन अभिक्रिया में हैलोऐल्केनों की तुलना में हैलोऐरीन कम क्रियाशील होते हैं।
(iii) स्वआयनन के फलस्वरूप हैलोऐरीनों से बना फेनिल धनायन अनुनाद के द्वारा स्थायी नहीं हो पाएगा। अतः SN1 क्रियाविधि की संभावना समाप्त हो जाती है।
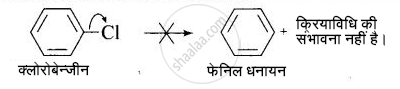
(iv) संभावित प्रतिकर्षण के कारण इलेक्ट्रॉनधनी नाभिकरागी के इलेक्ट्रॉनधनी ऐरीन की ओर जाने की संभावना कम होती है।
क्रियाशीलता को कैसे बढ़ाएँ:
ऑर्थो- तथा पैरा-स्थिति पर इलेक्ट्रॉन-अपनयक समूह (−NO2) उपस्थित होने पर हैलोऐरीन की क्रियाशीलता बढ़ जाती है।
जब −NO2 समूह ऑर्थो- तथा पैरा-स्थितियों पर जुड़ा होता है, तब यह प्रभाव अधिक प्रबल होता है। तथापि, इलेक्ट्रॉन अपनयक समूह के मैटा-स्थिति पर जुड़े होने की स्थिति में हैलोएरीनों की अभिक्रियाशीलता पर कोई प्रभाव प्रेक्षित नहीं होता है। अभिक्रिया की क्रियाविधि को निम्न प्रकार से आरेखित किया जा सकता है।
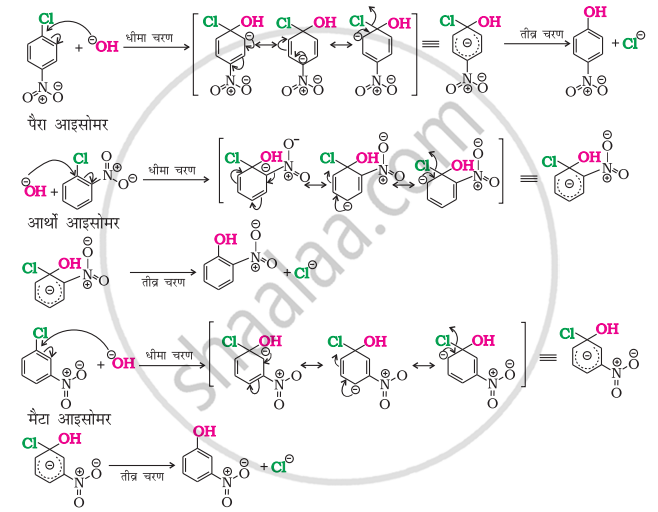
जैसा कि दर्शाया गया है, कि ऑर्थो- तथा पैरा-स्थिति पर नाइट्रो समूह को उपस्थिति से बेन्जीन वलय पर इलेक्ट्रॉन घनत्व कम हो जाता है। फलत: हैलोऐरीन पर नाभिकरागी का आक्रमण सरल हो जाता है।इस प्रकार बना कार्बऐनायन अनुनाद के द्वारा स्थायित्व प्राप्त कर लेता है। हैलोजन प्रतिस्थापी के स्थान से ऑर्थो- एवं पैरा-स्थितियों पर स्थित कार्बनों पर उत्पन्न ऋणावेश −NO2 के द्वारा स्थायित्व प्राप्त कर लेता है जबकि m-नाइट्रोक्लोरबेन्जीन में एक भी संरचना इस प्रकार की नहीं होती जिसमें −NO2 समूह कीउपस्थिति वाले कार्बन परमाणु पर ऋणावेश हो। अतः मेटा- स्थिति पर उपस्थित नाइट्रो समूह ऋणावेश को स्थायित्व प्रदान नहीं करता तथा मेटा- स्थिति पर उपस्थित −NO2 समूह का अभिक्रियाशीलता पर कोई प्रभाव प्रेक्षित नहीं होता।
APPEARS IN
संबंधित प्रश्न
निम्नलिखित में से किस अणु में तारांकित (*) कार्बन परमाणु असममित है?
(a) \[\begin{array}{cc}
\ce{H}\\
|\\
\phantom{.}\ce{C^*}\phantom{}\\
\phantom{}/\phantom{..}|\phantom{..}\backslash\phantom{}\\
\phantom{..}\ce{I}\phantom{...}\ce{Br}\phantom{.}\ce{Cl}\phantom{.}
\end{array}\]
(b) \[\begin{array}{cc}
\ce{D}\\
|\\
\phantom{.}\ce{C^*}\phantom{}\\
\phantom{}/\phantom{..}|\phantom{..}\backslash\phantom{}\\
\phantom{..}\ce{I}\phantom{...}\ce{Br}\phantom{.}\ce{Cl}\phantom{.}
\end{array}\]
(c) \[\begin{array}{cc}
\ce{H}\\
|\\
\phantom{.}\ce{C^*}\phantom{}\\
\phantom{}/\phantom{..}|\phantom{..}\backslash\phantom{}\\
\phantom{..}\ce{HO}\phantom{..}\ce{C2H5}\phantom{}\ce{CH3}\phantom{}
\end{array}\]
(d) \[\begin{array}{cc}
\ce{H}\\
|\\
\phantom{.}\ce{C^*}\phantom{}\\
\phantom{}/\phantom{..}|\phantom{..}\backslash\phantom{}\\
\phantom{....}\ce{H}\phantom{..}\ce{C2H5}\phantom{}\ce{CH3}
\end{array}\]
निम्नलिखित में से कौन-सी संरचना नीचे दिए अणु (A) का प्रतिबिंब रूप है?

क्लोरोबेन्जीन को AlCl3 की उपस्थिति में क्लोरीन की बेन्जीन से अभिक्रिया द्वारा बनाया जा सकता है। इस अभिक्रिया में निम्नलिखित में से कौन-सी स्पीशीज़ बेन्जीन बलय पर आक्रमण करती है?
सोडियम हाइड्रॉक्साइड के साथ C6H5CH2Br की अभिक्रिया ______ अग्रसारित होती है।
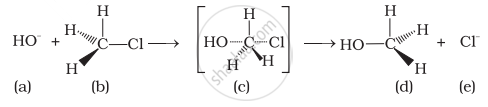
अभिक्रिया माध्यमिक के लिए निम्नलिखित में से कोन-से कथन सही हैं?
(i) माध्यमिक (c) अस्थायी है क्योंकि इसमें कार्बन पाँच परमाणुओं से जुड़ा है।
(ii) माध्यमिक (c) अस्थायी है क्योंकि इसमें कार्बन परमाणु sp2 संकरित है।
(iii) माध्यमिक (c) स्थायी है क्योंकि इसमें कार्बन परमाणु sp2 संकरित है।
(iv) माध्यमिक (c) अभिक्रियक (b) से कम स्थायी है।
निम्नलिखित यौगिकों में से कौन-सा यौगिक SN1 अभिक्रिया में –OH आयन से अधिक तेजी से अभिक्रिया करेगा?
\[\ce{CH3-CH2-Cl}\] अथवा \[\ce{C6H5-CH2-Cl}\]
हैलोऐरीन, हैलोऐल्केन और हैलोऐल्कीन से कम क्रियाशील होती हैं। समीक्षा कीजिए।
ऐलिल क्लोराइड n-प्रोपिल क्लोराइड की अपेक्षा अधिक आसानी से क्यों जलअपघटित होता है?
ऐल्किल हैलाइडों में निराकरण अभिक्रियाएँ (विशेषकर β-निराकरण) उतनी ही सामान्य हैं जितनी प्रतिस्थापन अभिक्रियाएँ। दोनों के अभिकर्मकों का उल्लेख कीजिए।
tert-ब्यूटिलब्रोमाइड जलीय NaOH के साथ SN1 क्रियाविधि से अभिक्रिया करता है, जबकि n-ब्यूटिलब्रोमाइड SN2 क्रियाविधि द्वारा अभिक्रिया करता है। क्यों?
सायनाइड आयन उभदंती नाभिकरागी के समान क्रिया करता है। जलीय माध्यम में यह किस छोर से प्रबल नाभिकरागी का कार्य करता है? अपने उत्तर का कारण दीजिए।
अभिकथन - KCN मेथिल क्लोराइड से अभिक्रिया करके मेथिल आइसोसायनाइड देता है।
तर्क - CN− एक उभदंती नाभिकरागी है।
अभिकथन - tert-ब्यूटिल ब्रोमाइड वुर्ट्ज अभिक्रिया द्वारा 2, 2, 3, 3-टेट्रामेथिलब्यूटेन देता है।
तर्क - वुर्टज अभिक्रिया में ऐल्किल हैलाइड शुष्क ईथर में सोडियम से अभिक्रिया करते हैं और हैलाइड में उपस्थित कार्बन परमाणुओं की संख्या से दुगनी संख्या वाला हाइड्रोकार्बन बनाते हैं।
अभिकथन - ऑर्थो और पैरा स्थितियों पर नाइट्रो समूह की उपस्थिति हैलोऐरीनों की नाभिकरागी प्रतिस्थापन के प्रति क्रियाशीलता बढ़ा देती है।
तर्क - नाइट्रो समूह इलेक्ट्रॉन अपनयक समूह होने के कारण बेन्ज़ीन वलय पर इलेक्ट्रॉन का घनत्व कम कर देता है।
अभिकथन - मोनोहैलोएरीनों में अगला इलेक्ट्रॉनरागी प्रतिस्थापन ऑर्थो और पैरा स्थितियों पर होता है।
तर्क - हैलोजन परमाणु वलय को निष्क्रिय करता है।
