Advertisements
Advertisements
प्रश्न
क्रिस्टल क्षेत्र विपाटन सिद्धांत का प्रयोग करते हुए ऊर्जा स्तर आलेख बनाइए और निम्नलिखित में केंद्रीय धातु परमाणु/आयन का इलेक्ट्रॉनी विन्यास लिखकर चुंबकीय आघूर्ण का मान निर्धारित कीजिए।
[FeF6]3–, [Fe(H2O)6]2+, [Fe(CN)6]4–
Advertisements
उत्तर
(1) [FeF6]3–:
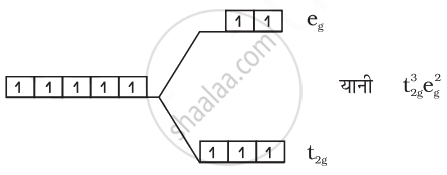
Fe3+ = 3d5
अयुगलित इलेक्ट्रॉनों की संख्या = 5
∴ चुंबकीय आघूर्ण = `sqrt("n"("n" + 2)) = sqrt(5(5 + 2))` = 5.92 BM
(2) [Fe(H2O)6]2+:
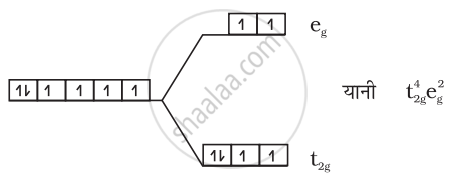
Fe2+ = 3d6
अयुगलित इलेक्ट्रॉनों की संख्या = 4
∴ चुंबकीय आघूर्ण = `sqrt("n"("n" + 2)) = sqrt(4(4 + 2))` = 4.9 BM
(3) [Fe(CN)6]4–:
Fe2+ = 3d6
CN− के प्रबल क्षेत्र लिगंड होने के कारण सभी इलेक्टॉन युगलित हो जाते हैं।
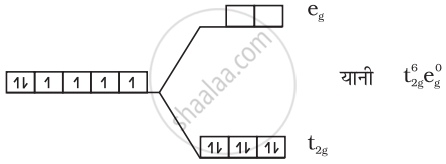
कोई अयुगलित इलेक्ट्रॉन नहीं है इसलिए प्रतिचुंबकीय।
APPEARS IN
संबंधित प्रश्न
उपसहसंयोजन यौगिकों का रंग क्रिस्टल क्षेत्र विपाटन पर निर्भर करता है। संकुलों [Co(NH3)6]3+, [Co(CN)6]3− तथा [Co(H2O)6]3+ का दृश्य क्षेत्र में तरंगदैर्घ्य के अवशोषण का सही क्रम क्या होगा?
[Fe(CN)6]3– संकुल के विषय में कौन-से विकल्प सही हैं?
(i) d2sp3 संकरण
(ii) sp3d2 संकरण
(iii) अनुचुंबकीय
(iv) प्रतिचुंबकीय
क्रिस्टल क्षेत्र विपाटन के आधार पर स्पष्ट कीजिए कि Co(III) दुर्बल क्षेत्र लिगंड के साथ अनुचुंबकीय अष्टफलकीय संकुल क्यों बनाता है जबकि प्रबल क्षेत्र लिगंड के साथ यह प्रतिचुंबकीय अष्टफलकीय संकुल बनाता है।
क्रिस्टल क्षेत्र विपाटन सिद्धांत के आधार पर निम्नलिखित संकुलों के इलेक्ट्रॉनिक विन्यास लिखिए।
CuSO4.5H2O का रंग नीला होता है जबकि CuSO4 रंगहीन होता है क्यों?
कॉलम I में दिए संकुल आयनों और कॉलम II में दिए संकरण तथा अयुगलित इलेक्ट्रॉनों की संख्या को सुमेलित कीजिए और सही कोड प्रदान कीजिए।
| कॉलम I (संकुल आयन) | कॉलम II (संकरण, अयुगलित इलेक्ट्रॉनों की संख्या) |
| (A) [Cr(H2O)6]3+ | (1) dsp2, 1 |
| (B) [Co(CN)4]2– | (2) sp3d2, 5 |
| (C) [Ni(NH3)6]2+ | (3) d2sp3, 3 |
| (D) [MnF6]4– | (4) sp3, 4 |
| (5) sp3d2, 2 |
अभिकथन: ([Fe(CN)6]3− आयन दो अयुगलित इलेक्ट्रॉनों के समकक्ष चुंबकीय आघूर्ण प्रदर्शित करता है।
तर्क - क्योंकि इसमें d2sp3 संकरण होता है।
संयोजकता आबंध सिद्धांत द्वारा [Co(NH3)6]3+ के संबंध में निम्नलिखित को स्पष्ट कीजिए।
- संकरण का प्रकार
- आंतरिक अथवा बाह्य कक्षक संकुल
- चुंबकीय व्यवहार
- केवल प्रचक्रण चुंबकीय आघूर्ण मान
संकुल का प्रेक्षित रंग संकुल द्वारा अवशोषित तरंग दैर्घ्य से कैसे संबधित होता है?
