Advertisements
Advertisements
प्रश्न
क्या आप एक जिंक के पात्र में कॉपर सल्फेट का विलयन रख सकते हैं?
Advertisements
उत्तर
\[\ce{E^Θ_{{Zn^{2+}/{ Zn}}}}\] = −0.76V; \[\ce{E^Θ_{{Cu^{2+}, { Cu}}}}\] = 0.34 V
अब हम यह जाँच करेंगे कि निम्नलिखित अभिक्रिया होगी अथवा नहीं।
\[\ce{Zn_{(s)} + CuSO4_{(aq)} -> ZnSO4_{(aq)} + Cu_{(s)}}\]
सेल को इस प्रकार प्रदर्शित किया जा सकता है –
\[\ce{Zn | Zn^{2+} || Cu^{2+} | Cu}\]
\[\ce{E^Θ_{{सेल}} = E^Θ_{{Cu^{2+}/{ Cu}}} - E^Θ_{{Zn^{2+},{ Zn}}}}\]
= 0.34 V – (– 0.76 V)
= 1.1 V
चूंकि \[\ce{E^Θ_{{सेल}}}\] धनात्मक है, अत: अभिक्रिया होगी तथा इस कारण हम जिंक के पात्र में कॉपर सल्फेट नहीं रख सकते हैं।
APPEARS IN
संबंधित प्रश्न
निम्नलिखित धातुओं को उस क्रम में व्यवस्थित कीजिए जिसमें वे एक-दूसरे को उनके लवणों के विलयनों में से प्रतिस्थापित करती हैं।
\[\ce{Al, Cu, Fe, Mg}\] एवं \[\ce{Zn}\]
निम्नलिखित में से किसी सेल के अक्रिय इलेक्टोड के विषय में कौन-सा कथन सही नहीं है?
एक विद्युत् रासायनिक सेल, विद्युत् अपघटनी सेल के समान व्यवहार कर सकता है जब _____।
दिए गए सेल, Mg | Mg2+ | | Cu2+ | Cu में ______ हैं।
(i) Mg कैथोड
(ii) Cu कैथोड
(iii) \[\ce{Mg + Cu^2+ -> Mg^2+ + Cu}\] सेल अभिक्रिया
(iv) Cu एक ऑक्सीकरण कर्मक
क्या किसी इलेक्टोड का परिशद्ध इलेक्टोड विभव मापा जा सकता है?
निम्नलिखित चित्र पर विचार कीजिए जिसमें एक विद्युत् रासायनिक सेल को एक विद्युत् अपघटनी सेल के साथ युगिमत किया गया है? विद्युत् अपघटनी सेल में इलेक्टोड 'A' तथा 'B' की ध्रुवणता क्या होगी?
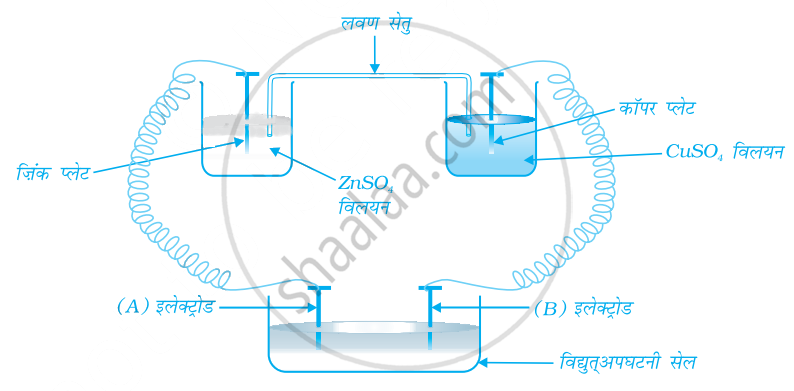
शुष्क सेल के विपरीत मर्करी सेल का सेल विभव अपनी सम्पूर्ण उपयोगी आयु में स्थिर क्यों रहता है?
नीचे दिए गए सेल पर विचार कीजिए-
Cu | Cu2+ | | Cl- | Cl2, Pt
ऐनोड व कैथोड पर होने वाली रासायनिक अभिक्रियाएँ लिखिए।
अभिकथन - किसी सेल द्वारा कार्य करने के लिए `"E"_"cell"` धनात्मक होना चाहिए।
तर्क- `"E"_"केथोड"` < `"E"_"एनोड"`
अभिकथन - मर्करी सेल स्थिर विभव नहीं देता।
तर्क - सेल अभिक्रिया में कोई आयन सम्मिलित नहीं होता।
