Advertisements
Advertisements
प्रश्न
प्लेटिनम इलेक्ट्रोड की उपस्थिति में CuSO4 के जलीय विलयन का विद्युत् अपघटन करने पर क्या होगा?
(i) कैथोड पर कॉपर निक्षपित होगा।
(ii) ऐनोड पर कॉपर निक्षिपित होगा।
(iii) ऐनोड पर ऑक्सीजन निकलेगी।
(iv) ऐनोड पर कॉपर घुलेगा।
Advertisements
उत्तर
(i) कैथोड पर कॉपर निक्षपित होगा।
(iii) ऐनोड पर ऑक्सीजन निकलेगी।
स्पष्टीकरण -
इलेक्ट्रोलिसिस के दौरान कैथोड पर निम्नलिखित प्रतिक्रिया होती है:
\[\ce{Cu^{2+} + 2e^{-} -> Cu}\]
\[\ce{H^{-} + 2e^{-} -> 1/2 H_2}\]
Cu2+/Cu की मानक इलेक्ट्रोड क्षमता `"H"^-/1/2 "H"_2` से अधिक है इसलिए Cu कैथोड पर जमा होगा।
APPEARS IN
संबंधित प्रश्न
चालकता सेल का सेल स्थिरांक ______.
दो विद्युत् अपघट्यों 'A' और 'B' के विलयनों को तनुकृत किया जाता है। 'B' का Λm1.5 गुना बढ़ता है जबकि A का Λm25 गुना बढ़ता है। इन दोनों में से कौन-सा प्रबल विद्युत् अपघट्य है? अपने उत्तर का औचित्य समझाइए।
डिस्चार्ज होते समय सीसा संचायक सेल में होने वाली अभिक्रिया लिखिए। जब बैटरी डिस्चार्ज होती है तो विद्युत् अपघट्य का घनत्व किस प्रकार प्रभावित होता है?
तनुता बढ़ाने पर CH3COOH के Λm का मान तेजी से क्यों बढ़ता है जबकि CH3COONa का Λm मान धीरे-धीरे से बढุता है?
कॉलम I तथा कॉलम II के मदों को सुमेलित कीजिए।
| कॉलम I | कॉलम II |
| (i) Λm | (a) मात्राविहीन गुण |
| (ii) `"E"_"cell"^⊖` | (b) आयनों की संख्या/आयतन पर निर्भर |
| (iii) κ | (c) विस्तीर्ण गुण |
| (iv) ΔrG | (d) तनुता के साथ बढ़ता है |
अभिकथन - विद्युत् अपघट्य विलयन को तनुकृत करने पर दुर्बल विद्युत् अपघट्यों के Λm के मान में तीव्र वुद्ध होती है।
तर्क - दुर्बल विद्युत् अपघट्यों के विलयन की तनुता बढाने से उनके वियोजन की मात्रा बढ़ती है।
अभिकथन - NaCl विलयन का विद्युत् अपघटन O2 के बजाए ऐनोड पर क्लोरीन देता है।
तर्क - ऐनोड पर ऑक्सीजन बनने के लिए अधिवोल्टता चाहिए।
अभिकथन - जब ECell = 0 होता है तो विद्युत् धारा प्रवाहित होनी बन्द हो जाती है।
तर्क - सेल अभिक्रिया का साम्य स्थापित हो जाता है।
अभिकथन - कॉपर सल्फ़ेट को ज़ंक पात्र में रखा जा सकता है।
तर्क - कॉपर की तुलना में जिंक कम सक्रिय होता है।
चित्र के आधार पर निम्नलिखित प्रश्न के उत्तर दीजिए।
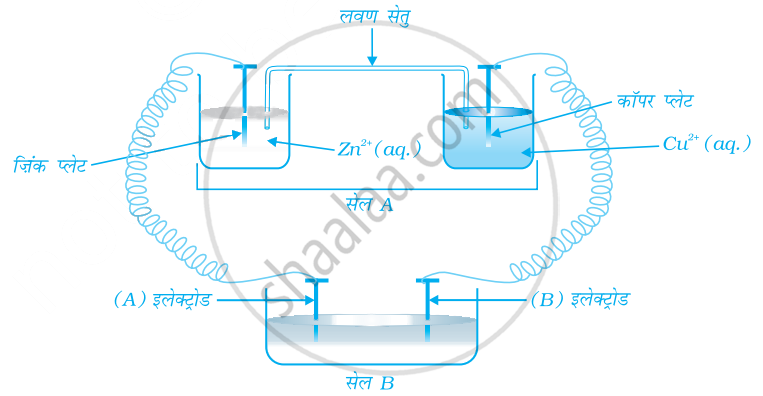
यदि सेल 'A' का Eसेल = 0.5 V तथा सेल 'B' का Eसेल = 1.1 V हो तो ऐनोड व कैथोड पर क्या अभिक्रियाएँ होगी?
