Advertisements
Advertisements
प्रश्न
HNH कोण का मान, HPH, HAsH तथा HSbH कोणों की अपेक्षा अधिक क्यों होता है?
(संकेत - NH3 में sp3 संकरण के आधार तथा हाइड्रोजन और वर्ग के दूसरे तत्वों के बीच केवल s-p आबंधन के द्वारा व्याख्या की जा सकती है।)
Advertisements
उत्तर
MH3 प्रकार के हाइड्राइडों में केंद्रीय परमाणु M इलेक्ट्रॉनों के तीन बंध युग्मों (bond pairs) तथा एक एकल युग्म (lone pair) से निम्न प्रकार से घिरा रहता है।
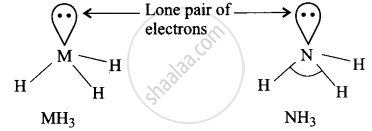
नाइट्रोजन परमाणु का आकार में बहुत छोटे तथा अधिक विद्युत ऋणात्मक होने के कारण NH3 में N परमाणु पर इलेक्ट्रॉन घनत्व का मान अधिकतम होता है। इस कारण बंध युग्मों के मध्य अधिकतम प्रतिकर्षण होता है और इस कारण HNH बंध कोण का मान अधिकतम होता है। परमाणु आकार में वृद्धि होने के कारण N से Bi की ओर जाने पर M की विद्युत ऋणात्मकता घटती है। फलस्वरूप इलेक्ट्रॉन युग्मों के मध्य प्रतिकर्षण कम हो जाता है। यही कारण है कि NH3 से BiH3 की ओर जाने पर H-M-H बन्ध कोण घटता है।
